中國粉體網訊 鈉硫電池是一種新型的電化學儲能電池,因其能量密度大、安全性高、壽命長、轉化效率高等優點引起廣大研究者的關注。鈉硫電池主要是由熔融態的正負極和β"-Al2O3固態電解質所組成,β"-Al2O3固態電解質起到隔離正負極和對鈉離子選擇性通過的雙重作用,避免正負極導通而短路,鈉離子在電池內部脫嵌移動從而產生電流。因此,β"-Al2O3固態電解質的好壞直接影響鈉硫電池的性能。目前,β"-Al2O3固態電解質制備工藝還不夠成熟,找到一種可行、適合、重復性好的制備工藝非常關鍵。
β"-Al2O3固態電解質陶瓷的制備包括粉體的合成、成型、燒結等諸多復雜的步驟。在粉體的合成方法上主要有固相合成法和液相合成法,固相合成法燒結溫度較高,其燒結溫度高于氧化鈉的熔點,高溫下長時間燒結使得氧化鈉揮發,導致β"-Al2O3的分解,且晶粒在高溫下燒結異常長大,導致粉末的不均勻性和雙重的相結構,這些對其離子電導率都是有害的。但固相反應法是制備β"-Al2O3最早、最普遍的方法之一,工藝簡單,成本較低且還可以起到對相的控制。
而液相合成法的反應物以分子形式均勻分散在水中,避免了固相反應中原子的長程擴散過程,可制的比表面積大、分散性好、反應活性高、顆粒和成分均勻的樣品,但其制備過程復雜,成本較高,產量小和不易控制等因素不利于工業化生產。因此開發出原料廉價、工藝流程簡單,并且結合新型制粉及燒結設備制備高性能β"-Al2O3前驅體粉末的工藝成為研究熱點。
中國鋁業鄭州有色金屬研究院車洪生高工認為勃姆石在鈉硫電池領域將會發揮重要作用。但據中國粉體網編輯查找近期文獻可知,目前這一領域的研究還不是很多。其中,西南科技大學的一篇碩士學位論文對此課題進行了較深入的研究。
研究者分別使用不同鋁源(α-Al2O3、(α+θ)-Al2O3和γ-AlOOH)、碳酸鈉和氧化鎂為原料固相合成法制備鎂穩定的β"-Al2O3粉末(由于β"相并非穩定相,需要添加一些添加劑來使其晶相穩定。國際上,通常采用Mg2+或Li+來穩定其β"相),在不同的溫度(1100℃-1700℃)煅燒2h,通過物相含量的計算、微觀結構、粒徑分布和熱重分析等測試方法,得出最優的固相法制備鎂穩定β"-Al2O3粉末的鋁源和合成溫度,為β"-Al2O3粉末的工業化生產提供借鑒意義。
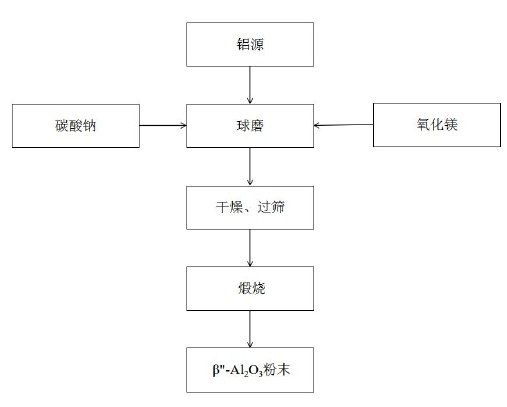
固相法合成β"-Al2O3粉末流程圖
實驗表明:以九水硝酸鋁和尿素200℃水熱制備的勃姆石(γ-AlOOH)為鋁源固相合成鎂穩定的β"-Al2O3粉末,在較低溫度下(1150℃)就能得到高純的β"-Al2O3粉末,其β"相含量達98.2%。在1150℃-1600℃之間,β"相保持相對穩定,沒有發生β"分解的現象,這比用α-Al2O3為鋁源固相合成鎂穩定的β"-Al2O3,其β"相含量高約15%。結合相純度和微觀粒徑的分布可知,1200℃-1300℃是較好的制備鎂穩定β"-Al2O3粉末的合成溫度。

不同原料的SEM圖:(a)γ-AlOOH(氫氧化鋁制);(b)γ-AlOOH(九水硝酸鋁制);(c)(α+θ)-Al2O3;(d)α-Al2O3

勃姆石(γ-AlOOH)為鋁源,不同溫度固相合成鎂穩定β"-Al2O3粉末掃描電鏡圖:(A)1200℃;(B)1300℃
此外,水熱合成勃姆石(γ-AlOOH)的兩類不同原料中,九水硝酸鋁和尿素水熱制備的勃姆石為鋁源固相合成鎂穩定的β"-Al2O3粉末,其β"相含量要高于用氫氧化鋁水熱制備勃姆石為鋁源固相合成鎂穩定的β"-Al2O3粉末。

氫氧化鋁在200℃不同水熱時間制備勃姆石的SEM圖:(a)0h;(b)3h;(c)4h;(d)5h;(e)6h;(f)7h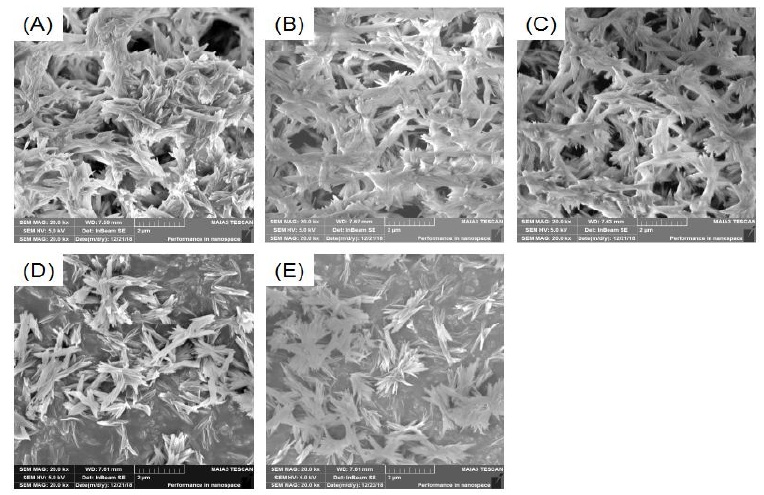
九水硝酸鋁和尿素在200℃不同水熱時間制備勃姆石的SEM圖:(A)1h;(B)2h;(C)3h;(D)4h;(E)8h
上述論文作者又繼續研究了用鎂穩定的β"-Al2O3粉體以傳統燒結和熱壓燒結來制備鎂穩定的β"-Al2O3陶瓷,比較兩種燒結方法對陶瓷體物相含量、微觀結構和離子電導率的影響,得出適合的陶瓷制備方法和較優的熱壓燒結參數。
【附:β"-Al2O3固態電解質的背景知識概述】
Na-beta-Al2O3固態電解質是一種超離子導體材料,也稱電解質陶瓷。其中,β-Al2O3和β"-Al2O3是beta-Al2O3兩個主要的子群,其經驗式分別為Na2O·11Al2O3和Na2O·5.33Al2O3。最初,beta-Al2O3被認為是氧化鋁的異質同構體。1926年,Stillwell闡明了β-Al2O3不是一種純物質,需要在氧化鋁中加入少量的鈉元素才能生成β-Al2O3。直到1931年,β-Al2O3的晶體結構才被Bragg等人使用X射線衍射所確定。隨后,Kummer和Yamaguchi等人發現了β-Al2O3另一種變體β"-Al2O3。由于β"-Al2O3的離子電導率要比β-Al2O3高,在制備β"-Al2O3時,希望得到較純的,不含其他雜質的β"-Al2O3,但研究發現,在Na2O-Al2O3二元系統中,β和β"相是同時存在的,Fally等人研究了此二元系統表明:在制備β"-Al2O3時,β和β"相在一定的溫度范圍內是共存的,且隨著溫度的上升,β生成更多的β"相,溫度上到一定的值時,隨著氧化鈉的揮發,β"相分解為β和α相,且這是一種不可逆的相變過程。
由于β"相并非穩定相,需要添加一些添加劑來使其晶相穩定。國際上,通常采用Mg2+或Li+來穩定其β"相,而MgO穩定的β"-Al2O3結構是由Bettman和Peter所確定的,其理想的化學式為Mg0.67Na1.67Al10.33O17。隨后,Bettman和Terner又發現了另一種新相β"'-Al2O3,確定其理想化學式為Mg1.88Na1.67Al14.96O25。而Weber等人在探究MgO-Na2O-Al2O3三元系統時,發現了β"相的另一種變體為Mg2.67Na1.67Al14.33O25,并命名為β"''-Al2O3。
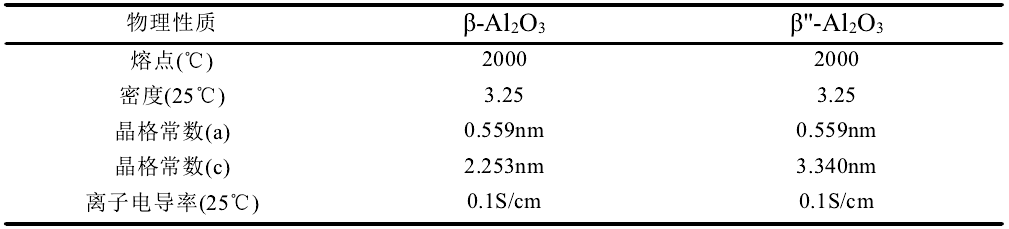
β/β"-Al2O3的物理性質
β"-Al2O3的晶體結構揭示出一價離子導電率高的原因。β"-Al2O3屬三方晶系,空間群為R-3m,晶格常數a為0.559nm,c為3.340nm,摻雜可能會引起其晶格常數的微小變化。β"-Al2O3是二維層狀結構導體,它的晶胞是由三個尖晶石基塊和三個鈉氧傳導層沿C軸交替排列,由于上下兩層尖晶石基塊中氧原子的排列不是鏡面對稱,所以β"-Al2O3晶胞不是關于鈉氧傳導層成鏡面對稱。尖晶石基塊中Al、O原子的排列和鎂鋁尖晶石晶格排列相類似,氧原子成立方密堆積排列,而鋁原子填在氧原子立方堆積的正四面體和正八面體中心,每個尖晶石基塊由四個氧原子層密堆積而成,每兩個相鄰的尖晶石基塊由鈉氧傳導層連接。在鈉氧傳導層上,由于氧原子排列不是很密集,且鈉離子半徑0.98nm比尖晶石基塊的晶格常數a(0.559nm)大,鈉原子只能在鈉氧的二維傳導層里移動,故β"-Al2O3的離子電導率呈各向異性。β-Al2O3屬六方晶系,空間群為P63/mmc,晶格常數a為0.559nm,c為2.253nm,其晶胞結構和β"-Al2O3相似,不同的是β-Al2O3晶胞是由兩個尖晶石基塊和兩個鈉氧傳導層交替排列構成,其中,相鄰兩個尖晶石基塊關于鈉氧層成鏡面對稱。由于β"-Al2O3的晶格常數c約為β-Al2O3的1.5倍,所以包含更多的鈉離子數,故β"-Al2O3的離子電導率高于β-Al2O3,因此是固態電解質首選的材料之一。
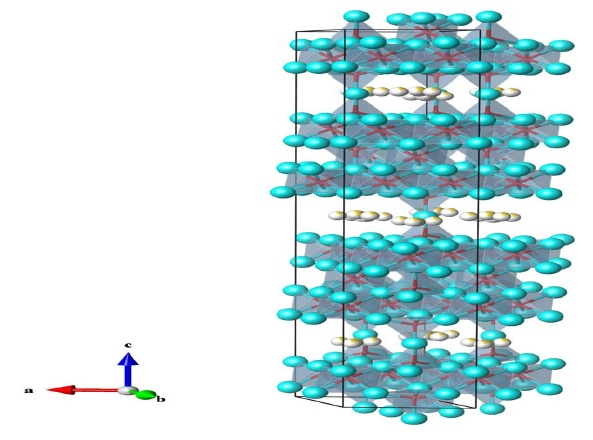
β"-Al2O3的晶胞
由于β"-Al2O3在高溫下極易分解為β和α相,雜相的存在會降低離子電導率,對固態電解質的電學性能有較大影響。實驗發現,引入一些摻雜離子可以使β"-Al2O3在高溫下穩定,不是所有的離子都能使β"-Al2O3達到穩定,只有那些摻雜離子的離子半徑小于0.097nm,才能進入尖晶石基塊和Al3+進行取代,從而達到穩定β"-Al2O3。由于摻雜離子的引入,一方面,添加離子可以和晶石基塊中的Al3+交換形成固溶體,也可以和鈉氧傳導層中的鈉離子進行取代,使得離子活化和定域在尖晶石基塊中。另一方面,異價的摻雜,使得正負電荷不相等,為了維持整個晶體的電荷守恒,必然會引入更多的缺陷和空位,使得鈉離子在二維傳導層遷移變得更加容易。這是摻雜對β"-Al2O3性能影響兩個方面的主要體現。
資料來源:
劉弟偉:β"-Al2O3固態電解質材料的制備和性能研究,西南科技大學
(中國粉體網編輯整理/平安)
注:圖片非商業用途,存在侵權告知刪除!